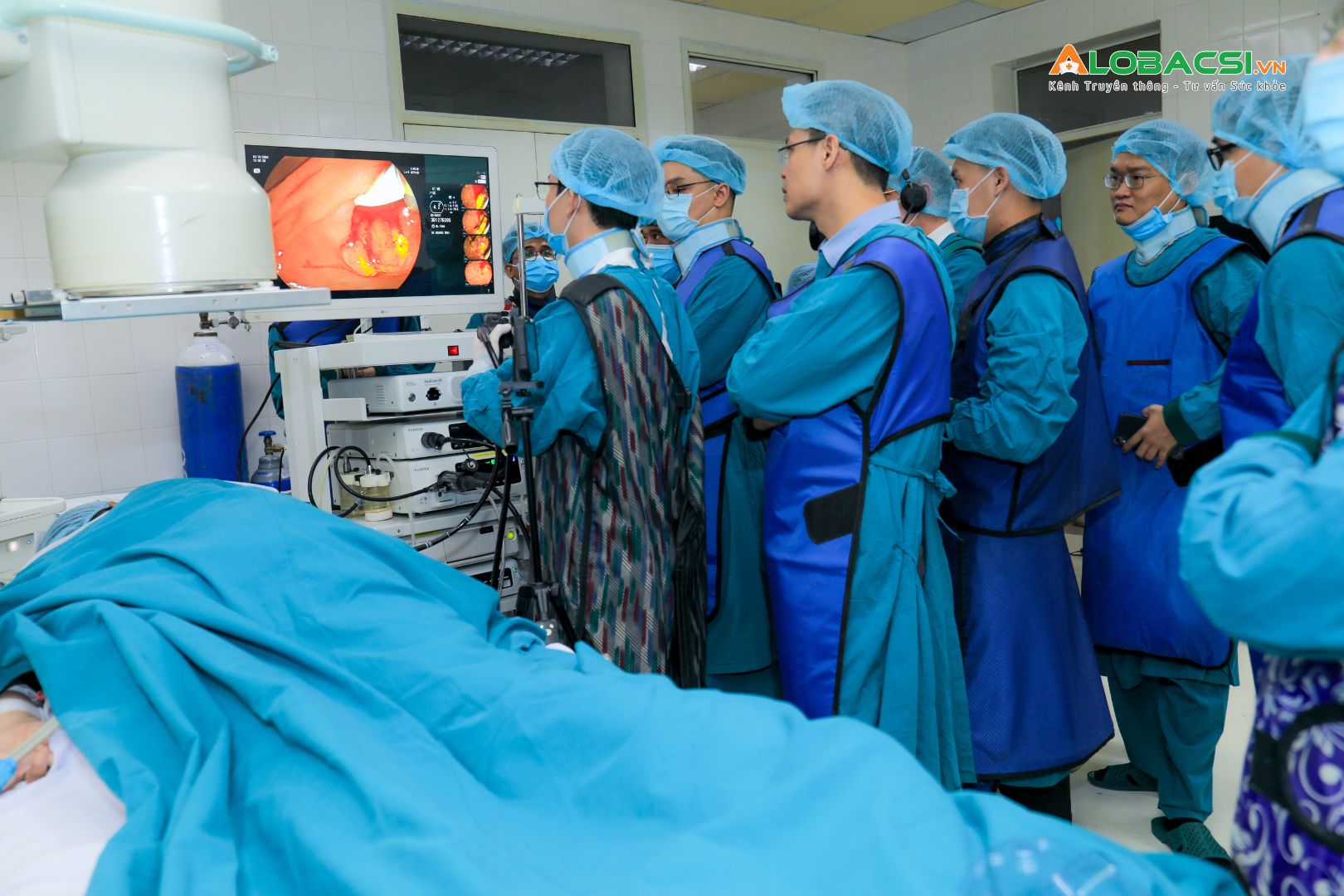
Bệnh nhân ung thư dạ dày có rất nhiều thuốc và cơ hội để điều trị
Đây là một trong những nội dung quan trọng được TS.BS Đoàn Thị Phương Thảo - Bệnh viện Đại học Y Dược TPHCM đề cập trong Hội nghị Khoa học Ngoại khoa và Phẫu thuật Nội soi toàn quốc 2024 (VASEL 2024) diễn ra vào ngày 22/11/2024, tại Bệnh viện Đại học Y Dược TPHCM.
Theo đó, TS.BS Đoàn Thị Phương Thảo - Bệnh viện Đại học Y Dược TPHCM cho biết, ung thư dạ dày (GC) thường gặp và có tỷ lệ tử vong cao (đứng hàng thứ ba do ung thư trên toàn cầu). Do chất lượng và khả năng tiếp cận để điều trị ung thư không bằng các nước phương Tây nên tỷ lệ tử vong ở vùng Đông Á vẫn cao hơn.
“Hiện nay, bệnh nhân ung thư có rất nhiều thuốc và cơ hội để điều trị. Tuy nhiên đây là bệnh lý không đồng nhất về hình thái trong chẩn đoán giải phẫu bệnh cho đến chẩn đoán phân tử nên việc xác định chính xác và lựa chọn phác đồ điều trị cho người bệnh là một thách thức.
Một trong những yếu tố quan trọng nhất là ung thư dạ dày phải được phân loại theo cấp độ phân tử, không chỉ phân loại mô bệnh học như từ trước đến nay” - TS.BS Đoàn Thị Phương Thảo nhấn mạnh.

Từ năm 1965 - 1990, mới bắt đầu có sự tiến bộ, trước đó chỉ chẩn đoán trên H&E và điều trị bằng phẫu thuật và hóa trị.
Đến thập niên 90, có hóa mô miễn dịch (IHC) và HER2 là dấu ấn sinh học đầu tiên để sử dụng thuốc điều trị nhắm trúng đích. Khi thế giới giải mã được toàn bộ bộ gen của con người là nền tảng để phát triển. Từ 1990 - 2014, đã có phân loại ung thư dạ dày ở mức độ phân tử.
Sau đó, ngày càng tiến bộ và nhận diện ra những dấu ấn sinh học như PD-L1, TMB,… cho đến hiện nay, từ đó có thuốc điều trị cho người bệnh.
TS.BS Đoàn Thị Phương Thảo đặc biệt lưu ý: “Với kỷ nguyên y học chính xác phải đúng bệnh nhân, đúng thuốc, đúng liều và đúng thời điểm. Chẩn đoán giải phẫu bệnh trễ sẽ không còn nhiều ý nghĩa đối với các bác sĩ”.
Hiện nay, các phân loại hình thái học ung thư dạ dày thường được ứng dụng: Một là Lauren classification (1965): ruột (intestinal type) và lan tỏa (diffuse type). Hai là Japanese Gastric Cancer Association (JGCA) classification (2017): vị trí, giai đoạn và đặc điểm mô bệnh học. Ba là WHO classification (2019): nhấn mạnh các đặc điểm mô bệnh học và subtypes.

Một trong những đặc tính có tiên lượng độc lập cho bệnh nhân là độ mô học gồm: biệt hóa rõ, biệt hóa vừa, biệt hóa kém (không tạo thành mầm móng). Tuy nhiên, khả năng ứng dụng lâm sàng hạn chế trong hướng dẫn điều trị chính xác cho từng bệnh nhân.
Từ năm 2014, phân loại phân tử của ung thư dạ dày theo TCGA dựa trên các đặc điểm phân tử và di truyền. Xây dựng nền tảng cho liệu pháp cá nhân hóa, đặc biệt trong việc lựa chọn liệu pháp nhắm đích và miễn dịch. Phân tích giải trình tự gen quy mô lớn đã chia 4 phân nhóm phân tử:
1. Dương tính với virus Epstein-Barr (EBV-positivity): 9%.
2. Bất ổn vi vệ tinh (Microsatellite Instability - MSI): 22%.
3. Khối u ổn định về mặt gen (Genomically Stable - GS): 20%.
4. Bất ổn nhiễm sắc thể (Chromosomal Instability - CIN): 49%.
Phân biệt các dấu ấn đối với ung thư dạ dày để có phác đồ trị liệu
TS.BS Đoàn Thị Phương Thảo cho biết, trong thực hành, các dấu ấn cần quan tâm đối với ung thư dạ dày để có phác đồ trị liệu cho người bệnh là HER2, MSI/MMR, PD-L1, TMB-H (gánh nặng đột biến cao), NTRK.
Đối với HER2, bác sĩ ung thư/ngoại khoa/nội soi tiêu hóa thu thập mẫu xét nghiệm đúng quy cách. Bác sĩ nội soi/phẫu thuật viên sinh thiết, định hướng, bảo quản mẫu mô trước khi gửi xét nghiệm. Sau đó, kỹ thuật viên giải phẫu bệnh xử lý mô và áp dụng phương pháp xét nghiệm chuẩn. Cuối cùng, bác sĩ giải phẫu bệnh đọc và trả lời kết quả.
Các nguyên nhân thay đổi kết quả HER2:
- Trước đánh giá: Thời gian đến khi phẫu tích và cố định, phương pháp xử lý mổ, thời gian cố định, chất cố định.
- Trong đánh giá: Chất lượng thiết bị, quy trình phòng xét nghiệm, năng lực của nhân viên, cách bộc lộ kháng nguyên, các hóa chất xét nghiệm, kiểm soát, các điều kiện xét nghiệm, sử dụng hình ảnh phân tích.
- Sau đánh giá: Đánh giá kết quả, các tiêu chuẩn đánh giá kết quả, các yếu tố cần trả lời, hệ thống cho điểm.
HER2 không đồng nhất là thách thức lớn trong chẩn đoán, cũng như đọc kết quả và xử lý kết quả, vì vậy không phải ai cũng đọc được mà cần có sự huấn luyện.

Đối với PD-L1, các thuốc ức chế PD-1/PD-L1 khôi phục chức năng miễn dịch của tế bào T và đã chứng minh hiệu quả trong điều trị nhiều loại ung thư.
Các yếu tố ảnh hưởng đến PD-L1 là thời gian và phương pháp cố định, số lượng tế bào u/mẫu sinh thiết phải trên 100. Đánh giá thủ công nhuộm PD-L1 bởi bác sĩ giải phẫu bệnh có thể dẫn đến sai sót về độ tái lập giữa các lần đánh giá. Các nghiên cứu gần đây cho thấy phương pháp phân tích hình ảnh kỹ thuật số tự động có độ chính xác và tính nhất quán.
Đối với MSI, đây là hiện tượng mất ổn định của các đoạn lặp lại ngắn trong DNA (microsatellites) do sự mất chức năng của hệ thống sửa chữa bắt cặp sai (MMR), dẫn đến sự xuất hiện các đoạn microsatellite có chiều dài khác thường so với DNA ban đầu.
MMR là hệ thống sửa chữa DNA trong chu kỳ tế bào, nhận biết và sửa các lỗi xảy ra trong quá trình sao chép DNA (lỗi bắt cặp sai, chèn/xóa nucleotide). Các gen chính tham gia trong hệ thống MMR là MLH1, MSH2, MSH6, PMS2..
MSI-H (High) chiếm 6,9 - 22,7% trong ung thư dạ dày và có 6 - 13% liên quan đến hội chứng Lynch. Đặc điểm lâm sàng: Tỷ lệ mắc các hơn ở nữ giới; Thường gặp ở người lớn tuổi; Thường gặp ở ung thư hang vị (distal stomach); Liên quan chặt chẽ với type ruột (intestinal type) theo Lauren; Phát hiện ở giai đoạn sớm và có tiên lượng tốt.
Thách thức trong đánh giá IHC-MMR: Hóa mô miễn dịch (IHC) bị ảnh hưởng bởi thời gian và hóa chất cố định. Các mẫu nhuộm có thể không xuất hiện đồng nhất, đôi khi xuất hiện nhuộm ở bào tương hoặc màng thay vì trong nhân.
Về tiêu chí đánh giá, mất biểu hiện được xác định là mất hoàn toàn < 1% tế bào. Lưu ý, IHC có tỷ lệ tương đồng cao với PCR (>90%) trong phát hiện MSI; IHC không rõ ràng, sử dụng PCR hoặc NGS để xác nhận trạng thái MMR.
Đối với TMB, được đo bằng tổng số đột biến soma mã hóa trên mỗi megabase (Mb) của bộ gen được giải trình tự, nếu càng nhiều thì đáp ứng hóa trị càng tốt. Nếu TMB cao (210 đột biến/Mb) là dấu ấn sinh học được sử dụng để lựa chọn bệnh nhân cho liệu pháp pembrolizumab. TMB có thể được kết hợp với các dấu ấn như MSI-H hoặc PD-L1 để tăng cường hiệu quả dự đoán.
Theo TS.BS Đoàn Thị Phương Thảo, quy trình giải phẫu bệnh bắt đầu từ phòng mổ: Thời gian trước cố định càng nhanh càng tốt (mẫu mô rời khỏi cơ thể, phân hủy ngay lập tức vì mất nguồn cung cấp máu và oxy, tích tụ các sản phẩm trao đổi chất, hoại sinh học và sự thối rữa do vi khuẩn).
Thời gian trong dung dịch cố định (6 - 8 giờ để định hình một mảnh mô 4mm): Ngăn chặn sự thối rữa và hoại sinh học; Giữ mô gần giống với mô bình thường; Làm cho tế bào không nhạy cảm với dung dịch ưu trương hoặc nhược trương; Đóng vai trò như một chất xúc tác cho thuốc nhuộm; Tạo ra sự tương phản hình thái tốt.
TS.BS Đoàn Thị Phương Thảo đặc biệt nhấn mạnh: “Tất cả các dấu ấn đều quan trọng và bệnh nhân dùng thuốc chi phí khá cao nên trách nhiệm của bác sĩ giải phẫu bệnh là đưa ra kết quả chính xác nhất để các nhà lâm sàng điều trị cho bệnh nhân tốt nhất”.
| Trong 3 ngày từ 21/11 - 23/11/2024, Hội Ngoại khoa và Phẫu thuật Nội soi Việt Nam phối hợp cùng Bệnh viện Đại học Y Dược TPHCM tổ chức Hội nghị Khoa học Ngoại khoa và Phẫu thuật Nội soi toàn quốc 2024 (VASEL 2024) với chủ đề “Chia sẻ tri thức - Định hình tương lai”, diễn ra tại TPHCM, quy tụ 428 chuyên gia trong và ngoài nước với hơn 500 bài báo cáo, gần 2.000 đại biểu tham dự. |
Bài viết có hữu ích với bạn?
Có thể bạn quan tâm
Đăng ký nhận bản tin sức khoẻ
Để chủ động bảo vệ bản thân và gia đình
Đăng ký nhận bản tin sức khoẻ để chủ động bảo vệ bản thân và gia đình